Какой объем 20%-ной серной кислоты плотностью 1.14 г/мл понадобился бы для растворения всего железа в исходной смеси? Тема задачи: Количество вещества. Моль. Молярная масса
Тема задачи: Количество вещества. Моль. Молярная масса
 Создано:
@evgeniya524
29 октября 2017
15:42
Создано:
@evgeniya524
29 октября 2017
15:42
Смесь железных и серебряных опилок обработали изб разб. HCl, при этом выделилось 4.48 л (н.у) H2. Какой объем 20%-ной кислоты серной кислоты плотностью 1.44 г/мл понадобился для растворения всего хлорида? Решения задачиAg+HCl реакция не идет Ag+H2SO4 реакция не идет Продолжение на рисунке 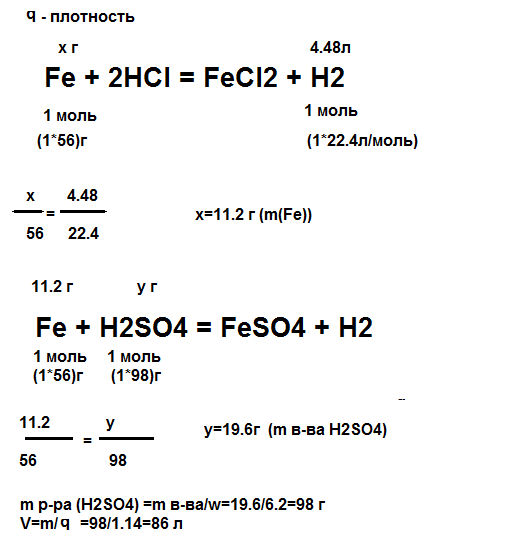
рисунок 1 КомментарииСмесь железных и серебряных опилок обработали избытком разбавленной соляной кислоты HCl, при этом выделилось 4.48 л (н.у) H2. Какой объем 20%-ной серной кислоты плотностью 1.14 г/мл понадобился бы для растворения всего железа в исходной смеси? Составляем пропорцию
$ \frac{11,2}{56} = \frac{y}{98} $ Откуда
$ y = \frac{11,2*98}{56} = 19,6 г в-ва H_{2}SO_{4} $ Находим какое количество 20% - ого раствора серной кислоты содержит 19,6 г г в-ва H_{2}SO_{4}. Составляем пропорцию
$ 100_{г р-ра} - 20_{г в-ва} $
$ x_{г р-ра} - 19,6_{г в-ва} $ или
$ \frac{x}{100} = \frac{19,6}{20} $ Откуда
$ x = \frac{100*19,6}{20} = 98 г р-ра $ Находим объем раствора серной кислоты
$ V = \frac{m}{q} = \frac{98}{1,14} = 86 мл $ Ответ: объем 20%-ой серной кислоты плотностью 1,44 г/мл равен
$ V = 86 мл $ КомментарииЧтобы предложить решение пожалуйста войдите или зарегистрируйтесь |
Записать новую задачу Все задачи Все темы Все химики |
Комментарии